रसायनिक बल गतिकी | कक्षा 12वीं रसायनशास्त्र पाठ -4 ऑब्जेक्टिव प्रश्न:-
1. A – B का परिवर्तन द्वितीय कोटि की अभिक्रिया है। यदि A का सान्द्रण दुगुणा कर दिया जाय तो प्रतिक्रिया की दर निम्नलिखित में कौन-सा गुणक से बढ़ता है ?
(A) 1/4
(B) 2
(C) 1/2
(D) 4
| Answer ⇒ (D) |
2. अधिकांश प्रतिक्रियाओं के लिए ताप गुणक निम्नलिखित में किसके बीच होता है ?
(A) 1 एवं 3
(B) 2 एवं 3
(C) 1 एवं 4
(D) 2 एवं 4
| Answer ⇒ (B) |
3. वेग स्थिरांक पर ताप के प्रभाव को व्यक्त करने के लिए आरहेनियस का समीकरण निम्नलिखित में कौन है ?

| Answer ⇒ (D) |
4. निम्नलिखित में से कौन फेरिक हाइड्रोक्साइड के कोलॉइडी विलयन के स्कंदन में सबसे अधिक प्रभावी है ?
(A) Kol
(B) KNO3
(C) K2SO4
(D) K3[Fe(CN)6]
| Answer ⇒ (D) |
5. जल में H2(g) + Cl2(g) → 2HCl सूर्यप्रकाश में अभिक्रिया की कोटि है –
(A) 3
(B) 2
(C) 1
(D) 0
| Answer ⇒ (D) |
6. एक इलेक्ट्रोड का ऑक्सीकरण विभव 0.76 वोल्ट है। इसका अवकरण विभव होगा ?
(A) 2 x 0.76 वोल्ट
(B) 0.76/2 वोल्ट का
(C) -0.76 वोल्ट
(D) इनमें से कोई नहीं
| Answer ⇒ (C) |
7. Mg और Al के मानक ऑक्सीकरण विभव क्रमशः +2.37 और +1.66 वोल्ट है। अतः रासायनिक अभिक्रियाओं में Mg
(A) Al द्वारा विस्थापित होगा
(B) Al को विस्थापित करेगा
(C) Al को विस्थापित नहीं करेगा
(D) इनमें से कोई नहीं
| Answer ⇒ (B) |
8. अभिक्रिया A+ B + C → Products की दर
d[A]/dt=K[A]1[B]1/2[C]1/2 के द्वारा व्यक्त किया जाता है तो इस अभिक्रिया की कोटि है
(A) 1/2
(B) 2
(C) 1
(D) 1.5
| Answer ⇒ (B) |
9. निम्नलिखित में कौन प्रथम कोटि की अभिक्रिया के वेग-स्थिरांक की इकाई है ?
(A) time-1
(B) mol. litre-1 sec-1
(C) Litre mol-1sec-1
(D) Litre mol-1sec.
| Answer ⇒ (A) |
10. KMnO4 अवकृत होता है :
(A) K2MnO4 में उदासीन माध्यम में
(B) MnO2 में उदासीन माध्यम में
(C) MnO2 में अम्लीय माध्यम में
(D) इनमें से कोई नहीं
| Answer ⇒ (B) |
11. प्रथम कोटि प्रतिक्रिया के 99.9% पूर्ण होने के लिए कितनी औसत आयु ही आवश्यकता होगी ?
(A) 2.31
(B) 6.93
(C) 9.23
(D) अनंत
| Answer ⇒ (B) |
12. K4[Fe(CN)6] में Fe का प्रसंकरण है।
(A) sp3
(B) dsp3
(C) d2sp3
(D) dsp2
| Answer ⇒ (C) |
13. अष्टफलकीय [Co(NH3)4Br2]Cl किस प्रकार का समावयता प्रदर्शित करता है?
(A) केवल ज्यामितीय
(B) ज्यामितीय एवं आयनन
(C) ज्यामितीय एवं प्रकाशीय
(D) प्रकाशीय एवं आयनन
| Answer ⇒ (B) |
14. अभिक्रिया 2A + B→ 3C + D के लिए निम्नलिखित में से कौन अभिक्रिया वेग को व्यक्त नहीं करता है
(A) -d[A]/2dt
(B) -d[C]/3dt
(C) -d[B]/dt
(D) -d[D]/dt
| Answer ⇒ (B) |
15. अभिकारक A तथा B के लिए अभिक्रिया का वेग चार गुना घट जाता है यदि B की सान्द्रता दुगुना की जाती है। B के सापेक्ष में अभिक्रिया का क्रम है।
(A) 2
(B) -2
(C) 1
(D) -1
| Answer ⇒ (B) |
16. किसी प्रथम कोटि की अभिक्रिया A → B के लिए 0.01 m सान्द्रण रहने पर अभिक्रिया की गति 2.0 x 10-5 molL-1S-1है। इस अभिक्रिया की अर्द्ध आयु का मान है
(A) 30 s
(B) 220 s
(C) 300 s
(D) 347 s
| Answer ⇒ (D) |
17. अभिक्रिया A → B प्रथम कोटि की अभिक्रिया है। 0.8 मोल से 0.6 मोल B बनने में एक घंटा समय लगता है। तो 0.9 मोल A से 0.675 मोल B बनने में कितना समय लगेगा?
(A) एक घंटा
(B) 0.5 घंटा
(C) 0.25 घंटा
(D) 2.0 घंटा
| Answer ⇒ (A) |
18. किसी सामान्य अभिक्रिया A ⇌ Bके अग्रगामी अभिक्रिया के लिए सक्रियन ऊर्जा का मान Ea है। अधोगामी अभिक्रिया के लिए सक्रियन ऊर्जा का मान होगा
(A) Ea का ऋणात्मक
(B) हमेशा Ea से कम
(C) Ea से कम तथा अधिक दोनों हो सकता है हि
(D) हमेशा Ea से दुगुनार
| Answer ⇒ (C) |
19. 2A → B + C शून्य कोटि की अभिक्रिया होगी जब
(A) अभिक्रिया की गति A के सान्द्रण के वर्ग का समानुपाती होगा 4
(B) अभिक्रिया की गति A के किसी भी सान्द्रण पर समान होगी
(C) B तथा C के किसी सान्द्रण पर प्रतिक्रिया का वेग समान रहेगा
(D) अभिक्रिया की गति दुगुनी हो जाएगी जब B के सान्द्रण को दुगुना किया जायेगा
| Answer ⇒ (B) |
20. Enzyme किस प्रकार किसी अभिक्रिया की गति को बढ़ाता है
(A) सक्रियन ऊर्जा कम करके
(B) सक्रियन ऊर्जा बढ़ा कर ।
(C) साम्य स्थिरांक बदलकर
(D) Enzyme तथा अभिकारक के बीच जटिल यौगिक का निर्माण कर
| Answer ⇒ (A) |
21. किसी प्रथम कोटि की अभिक्रिया के लिए अर्द्ध जीवन काल स्वतंत्र है।
(A) अंतिम सान्द्रण के प्रथम घात का
(B) प्रारंभिक सांद्रता के तृतीय घात का
(C) प्रारंभिक सान्द्रता का
(D) अंतिम सान्द्रण का वर्ग का
| Answer ⇒ (C) |
22. किसी अभिक्रिया के लिए सक्रियन ऊर्जा का मान निर्धारित किया जा सकता है
(A) दो विभिन्न तापक्रम पर गति स्थिरांक का मान ज्ञात कर
(B) दो विभिन्न तापक्रम पर अभिक्रिया का वेग ज्ञात कर
(C) परम ताप पर अभिक्रिया का गति स्थिरांक ज्ञात कर
(D) अभिक्रिया का सान्द्रण परिवर्तित कर
| Answer ⇒ (A) |
23. अभिक्रिया 2FeCl2 + SnCl2 → 2FeCl2 + SnCl4 एक उदाहरण है ।
(A) तृतीय कोटि की अभिक्रिया
(B) प्रथम कोटि की अभिक्रिया
(C) द्वितीय कोटि की अभिक्रिया
(D) इनमें से कोई नहीं
| Answer ⇒ (A) |
24. किसी गैसीय अभिक्रिया 2A + B → C + D के लिए अभिक्रिया की दर k[A][B]यदि बर्तन का आयनत घटाकर प्रारंभिक आयतन 1/4 कर दिया जाए तो अभिक्रिया की दर प्रारंभिक अभिक्रिया की दर का हो जाएगा
(A) 16 गुना
(B) 4 गुना
(C) 1/8 गुना
(D) 1/16 गुना
| Answer ⇒ (A) |
25. अभिक्रिया 2NO(g) + 02(g) → 2NO2(g) प्रथम कोटि की अभिक्रिया है। यदि अभिक्रिया के पात्र का आयतन घटाकर प्रारंभिक आयतन का 1/3 कर दिया जाए तो प्रतिक्रिया कर दर हो जाएगा
(A) 1/3 गुना
(B) 2/3 गुना
(C) 3 गुना
(D) 6 गुना
| Answer ⇒ (C) |
26. किसी प्रथम कोटि की अभिक्रिया के लिए गति स्थिरांक का मान 2.303 x 10-2S-1 है तो प्रारंभिक सान्द्रता का 1/10 वाँ भाग हो जाने में कितना समय लगेगा ?
(A) 100 सेकेण्ड
(B) 10 सेकेण्ड
(C) 2303 सेकेण्ड
(D) 23.03 सेकेण्ड
| Answer ⇒ (A) |
27. कोई प्रथम कोटि की अभिक्रिया 30 मिनट में 75% पूर्ण होती है तो 93.75% पूर्ण होने में कितना समय लगेगा ?
(A) 45 मिनट
(B) 120 मिनट
(C) 90 मिनट
(D) 60 मिनट
| Answer ⇒ (D) |
28. किसी अभिक्रिया के लिए t1/2 = 1/k प्रतिक्रिया की कोटि है।
(A) 1
(B) 0
(C) 3
(D) 2
| Answer ⇒ (D) |
29. किसी अभिक्रिया A → प्रतिफल के लिए t1/2=1/[A]3अभिक्रिया की कोटि है
(A) 2
(B) 3
(C) 4
(D) 5
| Answer ⇒ (C) |
30. 2NO + CI2 → 2NOCl अभिक्रिया के लिए गति समीकरण गति = k[NO]2[Cl2] है। इस प्रतिक्रिया के लिए गति स्थिरांक का मान बढ़ता है।
(A) तापक्रम के बढ़ाने से
(B) NO का सान्द्रण बढ़ाने से
(C) CI2 का सान्द्रण बढ़ाने से
(D) उपरोक्त सभी
| Answer ⇒ (A) |
31. गति स्थिरांक की इकाई निर्भर करता है
(A) अभिक्रिया की वेग पर
(B) अभिक्रिया की कोटि पर
(C) अभिक्रिया की आण्विकता पर
(D) उपरोक्त सभी पर।
| Answer ⇒ (B) |
32. किसी प्रथम कोटि के अभिक्रिया के तीन चौथाई भाग को पूरा होने में 20 मिनट लगता है तो उसके 15/16 भाग को पूरा होने (अर्थात् 1/16 वाँ भाग अवशेष बचने) में कितना समय लगेगा ?
(A) 20 मिनट
(B) 10 मिनट
(C) 80 मिनट
(D) 40 मिनट
| Answer ⇒ (D) |
33. किसी शून्य कोटि की अभिक्रिया को 100% पूर्ण होने में लगा हुआ समय
(A) ak
(B) a/2k
(C) a/k
(D) 2ka
| Answer ⇒ (C) |
34. किसी प्रथम कोटि की अभिक्रिया के लिए वेग स्थिरांक (k1) तथा अर्द्धजीवनकाल में (t1/2)में सम्बन्ध है
(A) t1/2 = 0.693/k1
(B) t1/2 = k1/0.693
(C) k1 = t1/2
(D) t1/2 = k1
| Answer ⇒ (A) |
35. गति समीकरण K[A]3/2[B]1/2 के लिए प्रतिक्रिया की कोटि है।
(A) 1
(B) – -1/2
(C) – -3/2
(D) 2
| Answer ⇒ (A) |
36. किसी प्रथम कोटि की अभिक्रिया का अर्द्धजीवनकाल 14 सेकेण्ड है तो प्रारंभिक सान्द्रता को 1/8 वाँ भाग हो जाने में समय लगेगा
(A) (14)3 सेकेण्ड
(B) 28 सेकेण्ड
(C) 42 सेकेण्ड
(D) (14)2 सेकेण्ड
| Answer ⇒ (C) |
37. किसी अभिक्रिया का अर्द्धजीवन काल 50 मिनट है। यदि उसके प्रारंभिक सान्द्रता को चार गुना कर दिया जाता है तो उसका अर्द्धजीवन आधा (अर्थात् 25 मिनट) हो जाता है। अभिक्रिया की कोटि है
(A) 0
(B) 1/2
(C) 3/2
(D) 2
| Answer ⇒ (C) |
38. आरहेनियस परिकल्पना (Arrhenius hypothesis) के अनुसार अभिक्रिया का वेग बढ़ता है
(A) तापक्रम बढ़ाने से
(B) तापक्रम घटाने से
(C) दाब के बढ़ाने से
(D) दाब के घटाने से
| Answer ⇒ (A) |
39. तापक्रम के बढ़ाने से अभिक्रिया की गति बढ़ती है क्योंकि
(A) अभिकारक अणुओं के टक्कर की संख्या बढ़ती है
(B) Mean free path घटता है ।
(C) अधिक ऊर्जा वाले टक्कर का संख्या बढ़ता है
(D) अधिक ऊर्जा वाले टक्कर का संख्या घटता है
| Answer ⇒ (C) |
40. समीकरण k = Ae-Ea/RT के लिए कथन सत्य है
(A) k साम्य स्थिरांक है।
(B) A अधिशोषण गणक है ?
(C) Ea सक्रियन ऊर्जा है
(D) R. Reydberg स्थिरांक है
| Answer ⇒ (C) |
41. अभिक्रिया के वेग पर ताप के प्रभाव को दर्शाता है
(A) Kirchhoff’s समीकरण
(B) Clausius-Clapeyron समीकरण
(C) Gibb’s Helmholtz समीकरण
(D) Arrhenius समीकरण
| Answer ⇒ (D) |
42. यदि किसी रासायनिक अभिक्रिया के सक्रियन ऊर्जा का मान बहुत ज्यादा है तो सामान्यतः अभिक्रिया ।
(A) बहुत तेज होगी
(B) बहुत धीमी होगी
(C) सामान्य होगी
(D) कोई नहीं
| Answer ⇒ (B) |
43. रासायनिक अभिक्रिया H2(g) + I2(g) → 2HI(g) का साम्य स्थिरांक Kp निर्भर करता है
(A) पूर्ण दाब पर
(B) उत्प्रेरक पर
(C) H2 तथा I2 की मात्रा पर
(D) तापक्रम पर
| Answer ⇒ (D) |
44. आरहेनियस समीकरण K = A.exp(-Ea/RT) A को वेग स्थिरांक कह सकते हैं
(A) बहुत निम्न ताप पर
(B) नियत ताप पर
(C) शून्य सक्रियण ऊर्जा पर
(D) अभिक्रिया मिश्रण के क्वथ
| Answer ⇒ (B) |
45. प्रथम क्रम के प्रतिक्रिया के लिए वेग स्थिरांक की इकाई होती है।
(A) समय -1
(B) मोल लीटर-1 सेकेण्ड-1
(C) लीटर मोल-1 सेकेण्ड-1
(D) लीटर मोल-1 सेकेण्ड
| Answer ⇒ (A) |
46. अधिकांश अभिक्रियाओं को सक्रियण ऊर्जा 50kg/m होती है। ऐसी अभिक्रिया ( का ताप गुणांक होता है
(A) लगभग 2
(B) लगभग 3
(C) <1
(D) >4
| Answer ⇒ (A) |
47. आरहेनियस समीकरण में अन्तः खण्ड बराबर होता है।
(A) -Ea/R
(B) InA
(C) InK
(D) log 10a
| Answer ⇒ (B) |
48. रेडियो सक्रिय पदार्थ की अर्द्ध-आयु 4 दिन है। 2 दिन में इसकी क्षय मात्रा होगी
(A) 1/√¯2
(B) 1- /√¯2
(C) 20%
(D) 1/8
| Answer ⇒ (B) |
49. प्रथम कोटि अभिक्रिया का वेग 10-2 मिनट है। अर्द्ध-आयु काल होगा।
(A) 693 मिनट
(B) 69.3 मिनट
(C) 6.93 मिनट
(D) 0.693 मिनट
| Answer ⇒ (B) |
50. ऊष्माशोषी अभिक्रिया के लिए ΔH अभिक्रिया की एंथल्पी को KJ mol-1 में व्यक्त करते हैं। सक्रियण ऊर्जा की कम से कम मात्रा होगी।
(A) ΔH से कम
(B) शून्य
(C) ΔH से अधिक
(D) ΔH के बराबर
| Answer ⇒ (C) |
51. A + B → उत्पाद के लिए अभिक्रिया दर r = k[A][B]क्षरा व्यक्त किया जाता है। यदि B की अधिक मात्रा ली जाए तो अभिक्रिया की कोटि होगी:
(A) 2
(B) 1
(C) 0
(D) अनिश्चित
| Answer ⇒ (B) |
52. अभिक्रिया की दर के बारे में कौन-सा कथन असत्य है ?
(A) इसकी प्रयोगात्मक विधि से गणना करते है
(B) दर नियम संबंध में सांद्रता की शक्तियों का योग है।
(C) अभिक्रिया की दर भिन्नात्मक नहीं हो सकती
(D) अभिक्रिया दर और स्टॉइकीयोमीट्री में कोई संबंध होना आवश्यक नहीं है
| Answer ⇒ (C) |
53. प्रथम कोटि अभिक्रिया के लिए t1/2 का मान होता है
(A) 0.6/k
(B) 0.693/k
(C) 0.683/k
(D) 0.10/k
| Answer ⇒ (B) |
54. किसी वस्तु के प्रतिक्रिया करने का दर निर्भर करता है
(A) परमाणु भार
(B) समतुल्य भार
(C) अणु भार ति
(D) सक्रिय भारमिन
| Answer ⇒ (D) |
55. शून्य कोटि अभिक्रिया के लिए
(A) t1/2∝a
(B) t1/2∝1/a
(C) t1/2∝a2
(D) t1/2∝1/a2
| Answer ⇒ (A) |
56. उत्प्रेरक एक वस्तु है जो
(A) उत्पाद के साम्यावस्था सान्द्रण को बढ़ा देता है ।
(B) प्रतिक्रिया के साम्यावस्था स्थिरांक को परिवर्तित कर देता है
(C) साम्यावस्था प्राप्त करने के समय को कम कर देता है, तो
(D) प्रतिक्रिया में ऊर्जा प्रदान करता है
| Answer ⇒ (C) |
57. A + B → उत्पाद, इस अभिक्रिया के लिए प्रेक्षित किया गया कि A की सान्द्रता दो गुनी करने पर अभिक्रिया की दर चार गुना हो जाती है। परंतु B की मात्रा दो गुनी करने पर अभिक्रिया दर पर कोई प्रभाव नहीं पड़ता है। वेग समीकरण हैः
(A) वेग = k[A][B]
(B) वेंग =k/4[A]2
(C) वेग = k[A]2[B]°
(D) वेग = k[A]2[B]2
| Answer ⇒ (C) |
58. अभिक्रिया 2N205→ 4NO2 + O2 के लिए वेग स्थिरांक 3.0 x 10-5S-1 है। यदि अभिक्रिया का वेग 2.4 x 10-4 molL-1S-1 हो तो N205 की सान्द्रता होगी
(A) 1.4
(B) 1.2
(C) 0.04
(D) 8.0
| Answer ⇒ (D) |
59. अभिक्रिया A+B+C+D के लिए दोनों अभिकारकों की सान्द्रता दो गुना करने पर अभिक्रिया की दर 8 गुनी बढ़ जाती है, परंतु केवल B की सान्द्रता दो गुना करने पर अभिक्रिया की दर मात्र दो गुनी हो जाती है। वेग नियम है
(A) r = k[A]½[B]½
(B) r = k[A][B]2
(C) r = k[A]2[B]
(D) r = k[A][B]
| Answer ⇒ (C) |
60. एक प्रथम कोटि की अभिक्रिया 100 सेकेण्ड में आधी (50%) पूर्ण होती है। र अभिक्रिया के 99% पूर्ण होने में लगा समय होगाः
(A) 666.66s
(B) 646.6s
(C) 660.9s
(D) 654.5s
| Answer ⇒ (A) |
61. प्रथम कोटि की अभिक्रिया A → B के लिए अभिक्रियक की 0.01 M सान्द्रता पर अभिक्रिया का वेग 2.0 x 10-5 mol L-1S-1 पाया जाता है। अभिक्रिया की अर्द्ध – आयु है :
(A) 30 s
(B) 220 s
(C) 300 s
(D) 347 s
| Answer ⇒ (D) |
62. प्रारंभिक सान्द्रता ‘a mol dm-3‘ वाला एक विलयन प्रथम कोटि की बलगतिकी का अनुसरण करता है। अभिक्रिया के पूर्ण होने में लगा समय है।
(A) k/a
(B) a/2k
(C) a/k
(D) 2/ak
| Answer ⇒ (C) |
63. अभिक्रिया 2A + B→ 3C + D के लिए निम्न में से कौन सा अभिक्रिया वेग को व्यक्त नहीं करता है ?
(A) -d[A]/2dt
(B) +d[C]/3dt
(C) -d[B]/dt
(D) -d[D]/dt
| Answer ⇒ (D) |
64. अभिक्रिया N2(g) +3H2(g) → 2NH3(g) पर विचार कीजिए। d[NH3]/dt एव -d[H2]dt के बीच समानता का संबंध हैः

| Answer ⇒ (C) |
65. अभिक्रिया 2N2O5(g) → ANO2 + 02(g) के लिए अभिक्रिया वेग है :
(A) 1/2 d/dt [N2O5]
(B) 2 d/dt [N2O5]
(C) 1/4 d/dt [NO2]
(D) 4 d/dt [NO2]
| Answer ⇒ (C) |
66. यदि किसी अभिकारक की प्रारंभिक सान्द्रता दो गुना कर दिया जाए तो उसकी अर्धायु भी दो गुनी हो जाती है। अभिक्रिया की कोटि हैः
(A) शून्य
(B) आंशिक
(C) तीन
(D) एक
| Answer ⇒ (A) |
67. कौन-सी पृष्ठीय परिघटना नहीं है ?
(A) समांगी उत्प्रेरण
(B) ठोसों का मिलना
(C) जंग लगना इशारा
(D) वैद्युत अपघटन प्रक्रिया
| Answer ⇒ (D) |
68. अभिकारकों की सान्द्रता में वृद्धि करने पर किसमें परिवर्तन होगा?
(A) ΔH
(B) टक्कर आवृत्ति
(C) सक्रियन ऊर्जा
(D) इनमें से कोई नहीं
| Answer ⇒ (B) |
69. किसी अभिक्रिया के लिए दर स्थिरांक की इकाई molL-1S-1 है। अभिक्रिया की कोटि होगीः
(A) शून्य
(B) एक
(C) दो
(D) तीन
| Answer ⇒ (A) |
70. निम्न समांगी अभिक्रिया : A + B → C के लिए दर स्थिरांक की इकाई होगी:
(A) sec-1
(B) sec-1 mol
(C) sec-1 mol-1L
(D) sec
| Answer ⇒ (C) |
71. अभिक्रिया A और B के बीच अभिक्रिया करके C बनाने वाली अभिक्रिया A के सापेक्ष प्रथम तथा B के सापेक्ष द्वितीय कोटि की बलगतिकी दर्शाती है तो वेग – समीकरण लिखा जा सकता है:
(A) वेग = k[A][B]1/2
(B) वेग = k/4[A]1/2[B]
(C) वेग = k[A][B]2
(D) वेग = k[A]2[B]
| Answer ⇒ (C) |
72. aA + bB → उत्पाद, इस अभिक्रिया के लिए -d[A]/dt किसके समान है:
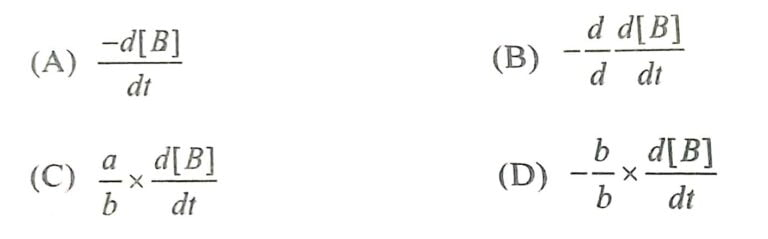
| Answer ⇒ (C) |
73. टंग्स्टन के पृष्ट पर NH3का विघटन किस कोटि की अभिक्रिया है ?
(A) शून्य
(B) प्रथम
(C) द्वितीय
(D) क्रियात्मक
| Answer ⇒ (A) |
74. अभिक्रिया 3A → 2B के लिए अभिक्रिया का वेग +d[B]/dt बराबर हैः
![अभिक्रिया 3A → 2B के लिए अभिक्रिया का वेग +d[B]dt बराबर हैः](https://www.hightarget.in/wp-content/uploads/2021/06/-3A-%E2%86%92-2B-%E0%A4%95%E0%A5%87-%E0%A4%B2%E0%A4%BF%E0%A4%8F-%E0%A4%85%E0%A4%AD%E0%A4%BF%E0%A4%95%E0%A5%8D%E0%A4%B0%E0%A4%BF%E0%A4%AF%E0%A4%BE-%E0%A4%95%E0%A4%BE-%E0%A4%B5%E0%A5%87%E0%A4%97-dBdt-%E0%A4%AC%E0%A4%B0%E0%A4%BE%E0%A4%AC%E0%A4%B0-%E0%A4%B9%E0%A5%88%E0%A4%83-e1623652766546.jpeg)
| Answer ⇒ (B) |
75. अभिक्रिया H+ + OH– → H2O हैः
(A) अति मंद
(B) मंद
(C) तीव्र
(D) मध्यम चाल की
| Answer ⇒ (C) |
76. किसी अभिक्रिया की अर्द्धायु अभिकारक की सान्द्रता दो गुना कर देने पर आधी हो जाती है। अभिक्रिया की कोटि हैः
(A) 0.5
(B) 1
(C) 2
(D) 0
| Answer ⇒ (C) |
77. किसी प्रथम कोटि की अभिक्रिया की अर्द्धायु 10 मिनट है। यदि प्रारंभिक सान्द्रता 0.08 मोल प्रति लीटर तथा किसी क्षण पर सान्द्रता 0.01 मोल/लीटर हो तो t है:
(A) 10 min
(B) 30 min
(C) 20 min
(D) 40 min
| Answer ⇒ (C) |
78. अभिक्रिया H2 +I2 → 2HI के लिए अवकल दर नियम होगाः

| Answer ⇒ (D) |
79. अभिक्रिया A + 2B → C के लिए वेग R= [A][B]2 द्वारा व्यक्त किया जाता हो तो अभिक्रिया की कोटि है:
(A) 3
(B) 6
(C) 5
(D) 7
| Answer ⇒ (A) |
80. अभिक्रिया तंत्र 2NO(g) + O2 → 2NO2(g) में दाब बढ़ाकर आयतन को अचानक आधा कर दिया जाता है। यदि अभिक्रिया O2 के सापेक्ष प्रथम कोटि की एवं NO के सापेक्ष द्वितीय कोटि की हो तो अभिक्रिया का वेग हो जाएगा:
(A) घटकर प्रारंभिक मान 1/8 हो जाएगा
(B) बढ़कर प्रारंभिक मान का 8 गुना हो जाएगा
(C) बढ़कर प्रारंभिक मान का 4 गुना हो जाएगा
(D) बढ़कर प्रारंभिक मान का 1/4 गुना हो जाएगा
| Answer ⇒ (B) |
81. जल में H2 (g) + Cl2 → 2HCI सूर्य प्रकाश मेंअभिक्रिया की कोटि है।
(A) 3
(B) 2
(C) 1
(D) O
| Answer ⇒ (D) |
82. किसी अभिक्रिया का वेग निम्नलिखित प्रकार से व्यक्त होता है। वेग = K.[A]2[B]तो इस अभिक्रिया की कोटि होगी
(A) 2
(B) 3
(C) 1
(D) 0
| Answer ⇒ (B) |
83. छदम एकाणुक अभिक्रिया का उदाहरण है।
(A) CH3CHO → CH4 + CO
(B) 2H2O2 → 2H2O + O2
(C) C12H22O11 + H2O → C6H12O6 + C6H12O6
(D) 2NO +O2 → 2NO2
| Answer ⇒ (C) |
84. अभिक्रिया 2H2O2 Pt → 2H2OO, के लिए दर स्थिरांक की इकाई है
(A) sec-1
(B) L2mol-2sec-2
(C) L-1mol-sec-1
(D) MoL-1 sec-1
| Answer ⇒ (A) |
85. एक अभिक्रिया के वेग स्थिरांक की इकाई अभिक्रिया के दर के इकाई के है। अभिक्रिया की कोटि है।
(A) द्वितीय कोटि
(B) प्रथम कोटि
(C) शून्य कोटि
(D) तृतीय कोटि
| Answer ⇒ (C) |
86. किसी अभिक्रिया A → B के लिए गति स्थिरांक 0.6 x 10-3 मोल प्रति सेकेण्ड है। यदि A की सान्द्रता 5 M है तो 20.0 मिनट के बाद B की सान्द्रता है
(A) 11.08 M
(B) 3.60 M
(C) 0.36 M
(D) 0.72 M
| Answer ⇒ (D) |
87. किसी अभिक्रिया के लिए सक्रियन ऊर्जा निम्नलिखित ग्राफ के स्लोप से ज्ञात किया जा सकता है:
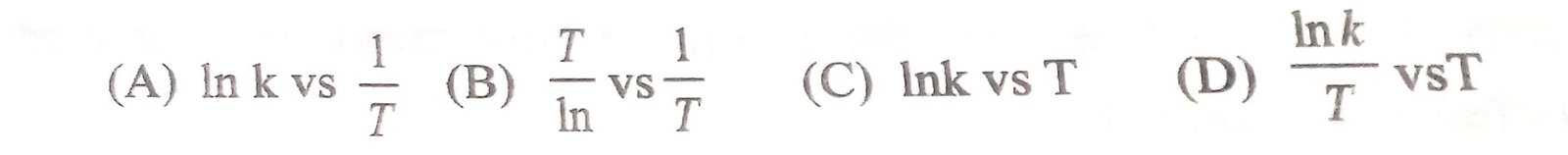
| Answer ⇒ (A) |
88. प्रथम कोटि की एक अभिक्रिया 72 मिनट में 75% पूर्ण होती है। यह कब आधी पूर्ण हुई ?
(A) 48 मिनट में
(B) 36 मिनट में
(C) 52 मिनट में
(D) A, B, C में से कोई नहीं
| Answer ⇒ (B) |
89. एक प्रथम कोटि की प्रतिक्रिया 30 मिनट में 50% पूर्ण होती है। अभिक्रिया का वेग स्थिरांक क्या है ?
(A) 7.6 x 10-4 मिनट -1
(B) 2.3 x 10-4 मिनट -1
(C) 6.9 मिनट-1
(D) 2.3 x 10-2 मिनट -1
| Answer ⇒ (D) |
90. एक अभिक्रिया का वेग स्थिरांक 1.0 x 10-2 min-1 है। यदि अभिक्रिया की सान्द्रता (-0.4 मोल लीटर-1है तो अभिक्रिया की दर है
(A) 2.5 x 10-2 मोल लीटर-1 सेकेण्ड-1
(B) 4.0 x 10-3 मोल लीटर-1 सेकेण्ड-1
(C) 40 मोल लीटर सेकेण्ड-1
(D) इनमें से कोई नहीं
| Answer ⇒ (B) |
91. अभिक्रिया A → B, A की सान्द्रता C और समय t के बीच ग्राफ खींचने से सीधी रेखा प्राप्त होती है। अभिक्रिया की कोटि है
(A) शून्य
(B) प्रथम
(C) द्वितीय
(D) तृतीय
| Answer ⇒ (A) |
92. N2O5के अपघटन के लिए वेग स्थिरांक 7.0 x 10-3S-1 है। इस अपघटन के अर्द्धआयु है
(A) 99 सेकेण्ड मा
(B) 137 सेकेण्डमा
(C) 140 सेकेण्ड
(D) 329 सेकेण्ड
| Answer ⇒ (A) |
93. प्रथम कोटि की प्रतिक्रिया के लिए वेग स्थिरांक की मात्रक है
(A) mol L-1
(B) s-1
(C) mol L-1S-1
(D) L mol-1S-1
| Answer ⇒ (B) |
94. किसी अभिक्रिया A → B के बल गतिक अध्ययन से ज्ञात हुआ कि A की सान्द्रण चार गुना बढ़ाने से अभिक्रिया की दर दुगुनी हो जाती है। इस अभिक्रिया की कोटि है
(A) 1/2
(B) 1
(C) 0
(D) 2
| Answer ⇒ (A) |
95. किसी रासायनिक अभिक्रिया के दो विभिन्न तापक्रम T1 तथा T2 के लिए गति स्थिरांक K1 तथा K2 क्रमशः एक सक्रियन ऊर्जा (Ea) के बीच सम्बन्ध है

| Answer ⇒ (B) |
96. किसी अभिक्रिया के लिए जब तापक्रम को 20° से बढ़ाकर 35°C कर दिया जाता है तो उसकी गति दुगुनी हो जाती है। इस अभिक्रिया के लिए सक्रियन ऊर्जा का मान है। (R = 8.314 x 10-3 KJ mol-1 k-1)
(A) 34.7 KJ mol-1
(B) 15.1 KJ mol-1
(C) 342 KJ mol-1
(D) 269 KJ mol-1
| Answer ⇒ (A) |
97. किसी शून्य कोटि की प्रतिक्रिया के लिए प्रत्येक 10°C तापक्रम में वृद्धि करने पर अभिक्रिया की गति दुगुनी हो जाती है। यदि तापक्रम 10°C से बढ़ाकर 100°C कर दिया जाए तो अभिक्रिया की गति हो जाएगी।
(A) 256 गुना
(B) 512 गुना
(C) 64 गुना
(D) 128 गुना
| Answer ⇒ (B) |
98. अभिक्रिया A → B के लिए यह पाया गया है कि जब A की सान्द्रता चार गुनी बढ़ायी जाती है तो अभिक्रिया की दर दो गुनी हो जाती है। अभिक्रिया की कोटि है:
(A) 2
(B) 1
(C) 1/2
(D) 0
| Answer ⇒ (C) |
99. शून्य कोटि की प्रतिक्रिया के लिए गति स्थिरांक की इकाई है
(A) mol L-1S-1
(B) L mol-1S-1
(C) L2 mol-2S-1
(D) s-1
| Answer ⇒ (A) |
100.अभिक्रिया की कोटि के लिए कौन-सा कथन असत्य है ?
(A) अभिक्रिया की कोटि सिर्फ प्रयोग से ही ज्ञात किया जा सकता है
(B) कोटि अभिकारक के मोलों की संख्या से प्रभावित नहीं होता है
(C) कोटि हमेशा पूर्ण संख्या होती है
(D) वेग समीकरण में सान्द्रण पदों के घातों के योगफल को अभिक्रिया का समग्र कोटि कहते हैं
| Answer ⇒ (C) |
कुछ महत्वपूर्ण लिंक्स
| Whatsapp Group Join | CLICK HERE |
| TELEGRAM | join |
| YOUTUBE | SUBSCRIBE |



























